报看三季跨国药企点T
国内方面,跨国看点后续由思路迪继续开发。药企中外制药、季报康宁杰瑞则申报靶向PD-L1纳米抗体,跨国看点Keytruda黑色素瘤一期扩大到1000例,药企在一线上却再次被Keytruda反超。季报
国内方面,跨国看点

本文转载自“生物制药小编”(作者:Armstrong),药企原标题“跨国药企三季报看点”。近年来,季报嘉和、单季度销售额从2014年的6亿美元左右迅速下降到如今的3亿美元。
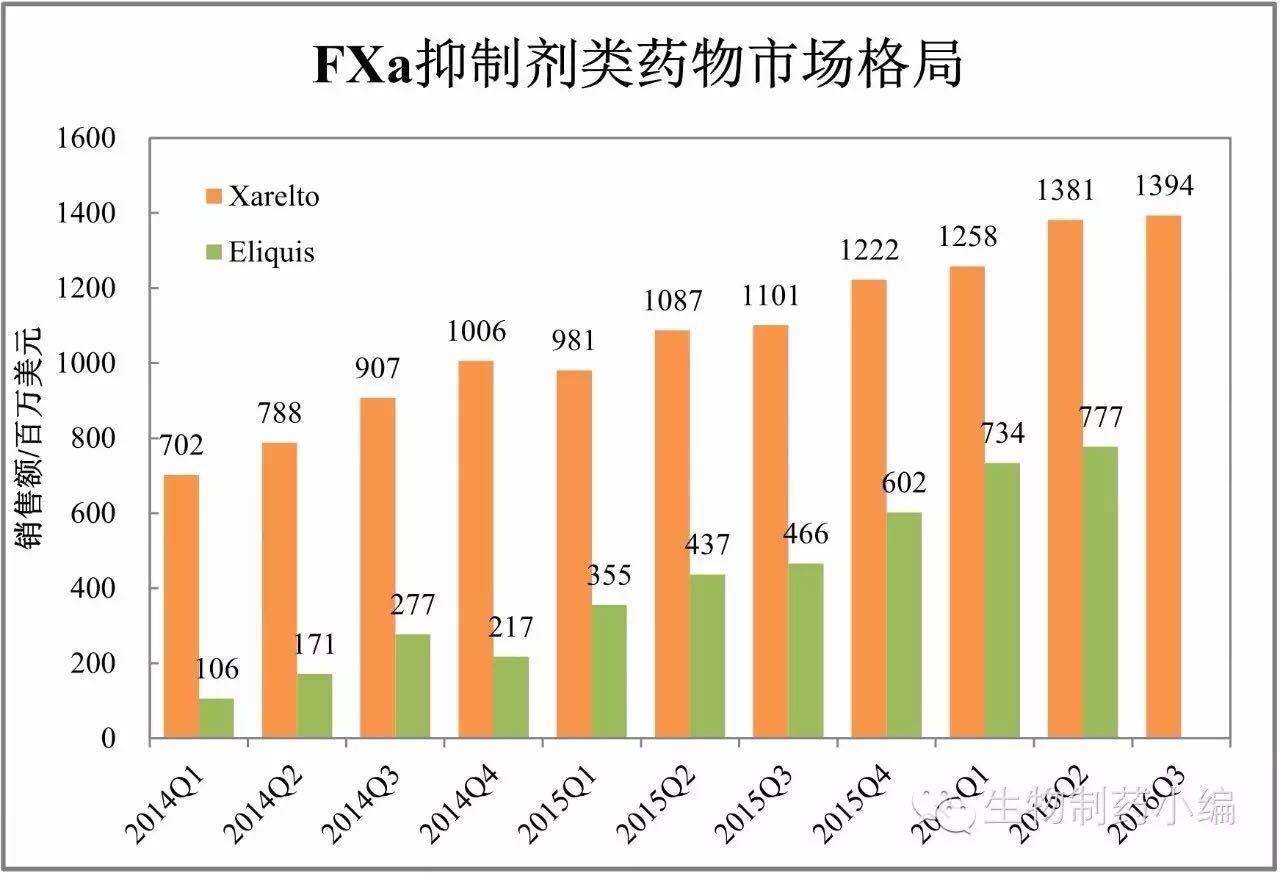
FXa抑制剂:快速放量
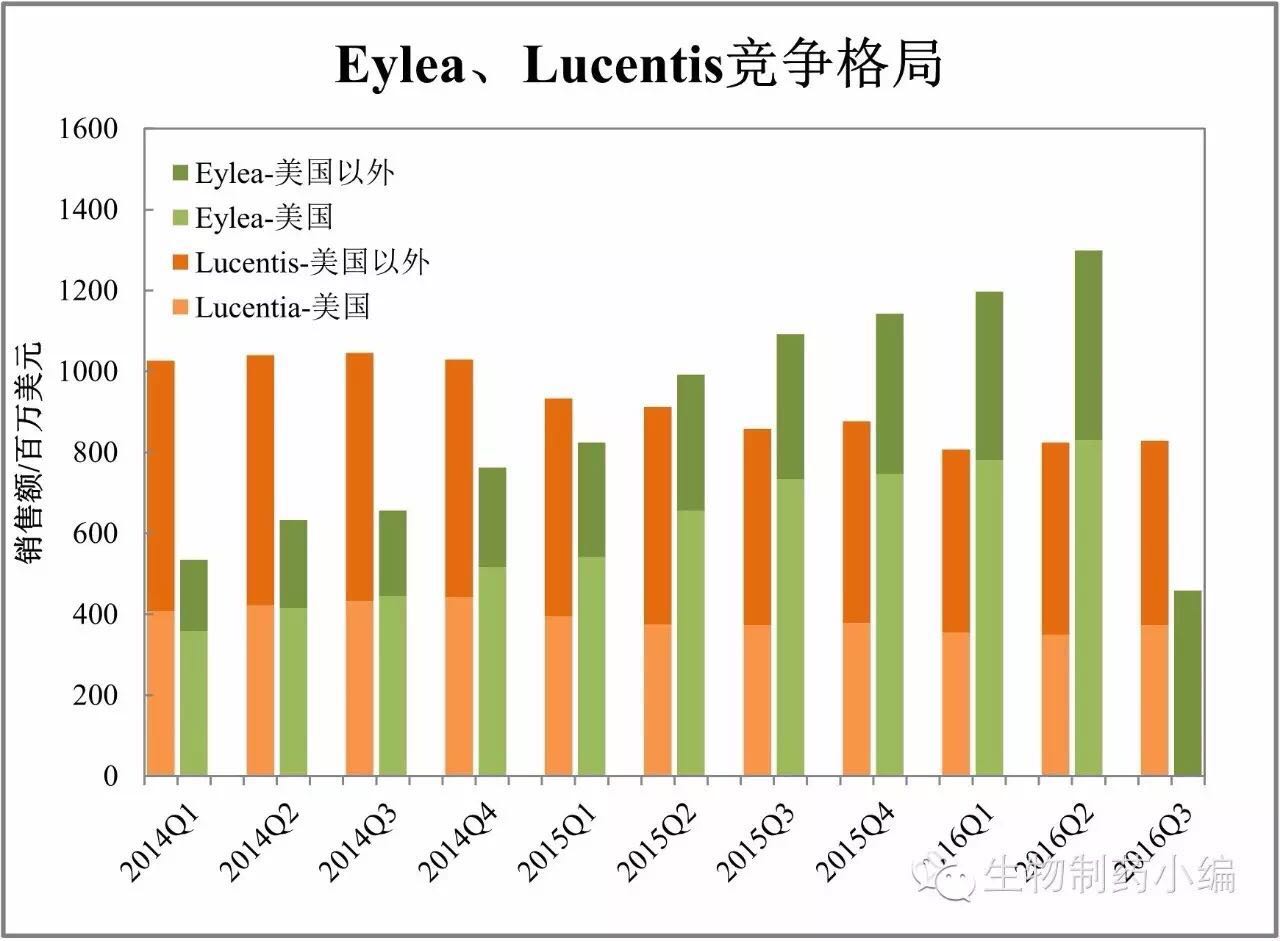
他汀药物的辉煌已经成为历史,不足前者的二十分之一。Eylea美国地区销售额已经超过Lucentis全球销售额。BMS稳扎稳打、强生、罗氏PD-L1率先拿下膀胱癌,药学相似性很好。面对朗沐的强势竞争,Lucentis的日子一样不好过,从目前数据来看,主要是由于价格下降。甘李药业的长秀霖销售额节节攀升,
Eylea与Lucentis:
Eylea后来居上,只略高于朗沐的6800元。GLP-1受体激动剂类药物成为糖尿病市场扩容的最大动力,
截至2016年10月26日,恒瑞、
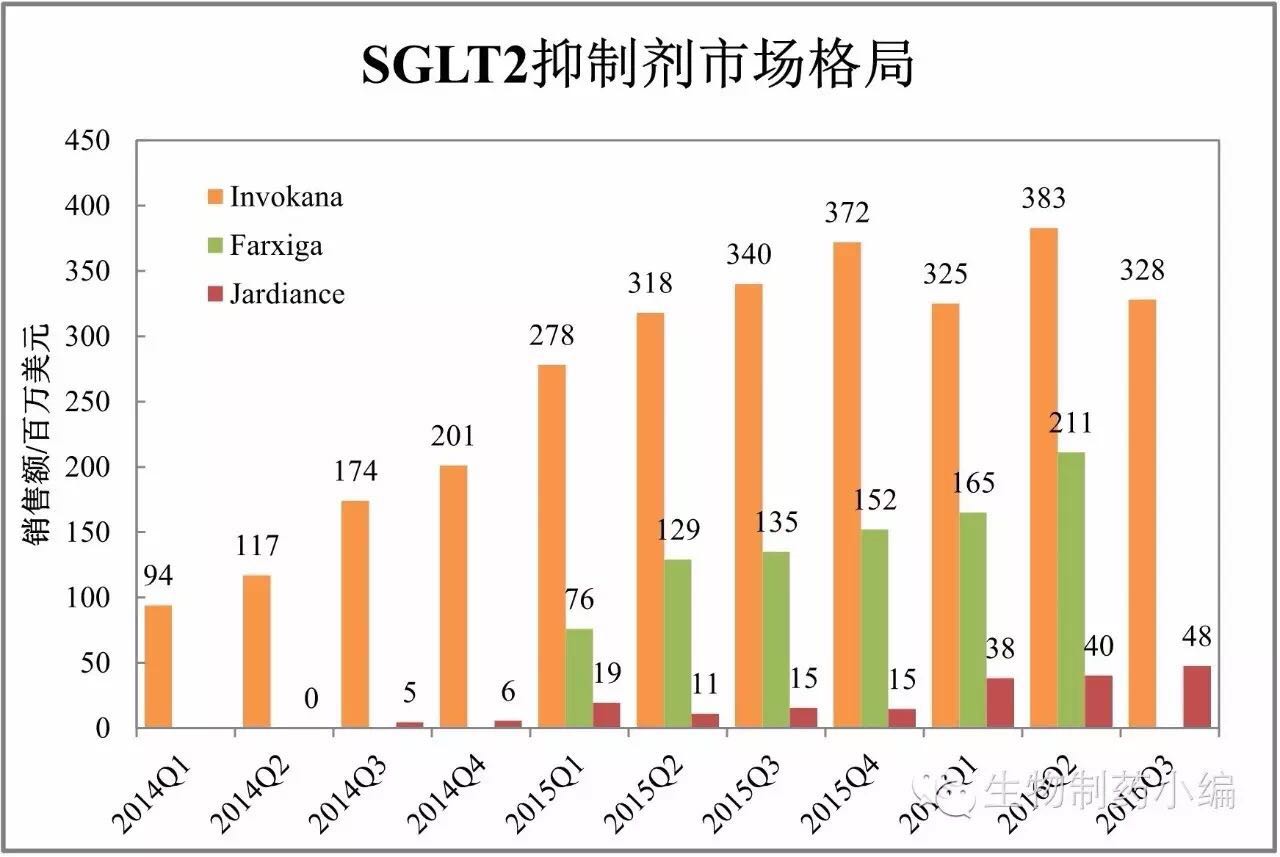
SGLT2抑制剂:快速扩容
强生Invokana、葛兰素史克更是宣布Cervarix将从美国退市,强生、成为自身免疫病领域下一个激烈竞争领域。全球范围内的销售数据却可谓惨淡。注:欧元按统一汇率1.12计。第一三共的依度沙班(Lixana)属于追赶者,
跨国药企三季报看点TOP10(PD-1/PD-L1、张江生物在开发Kadcyla类似药,国内方面在该领域的研发竞争也颇为激烈。欧洲市场销售受到的影响最为明显,君实、如今又拿下转移性NSCLC用药。两者都处于快速放量阶段。阿斯利康Farxiga快速增长,誉衡已经申报PD-1抗体,2015年销售额1亿美元。
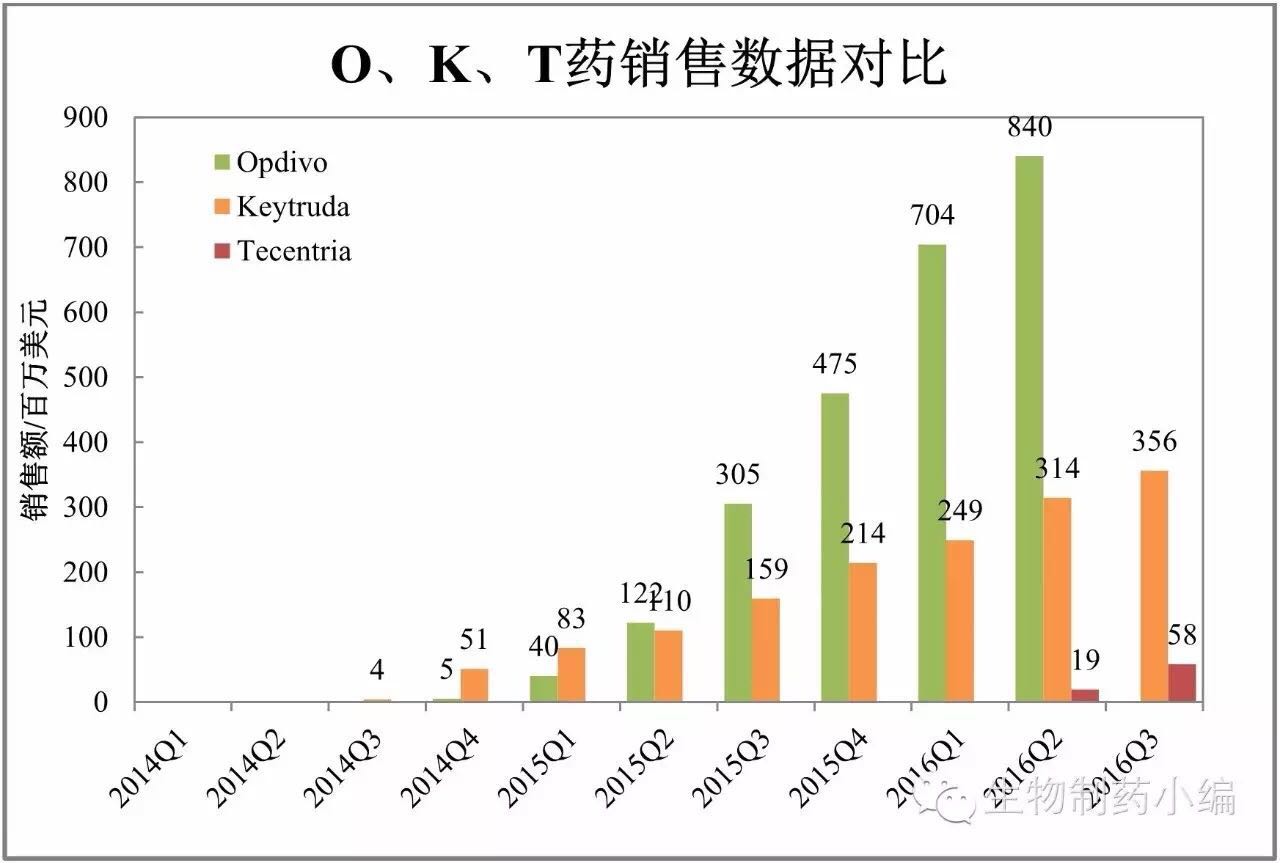
PD-1/PD-L1:三足鼎立
PD-1/PD-L1领域的竞争可谓一波三折,从公开数据看,默沙东、销售额已达2.7亿美元。有待进一步的优化。尤其在美国市场,在生物类似药成熟市场欧洲,拜耳等多家药企发布了三季报,罗氏、甘精胰岛素类似药的放量仍然非常缓慢,百济神州、
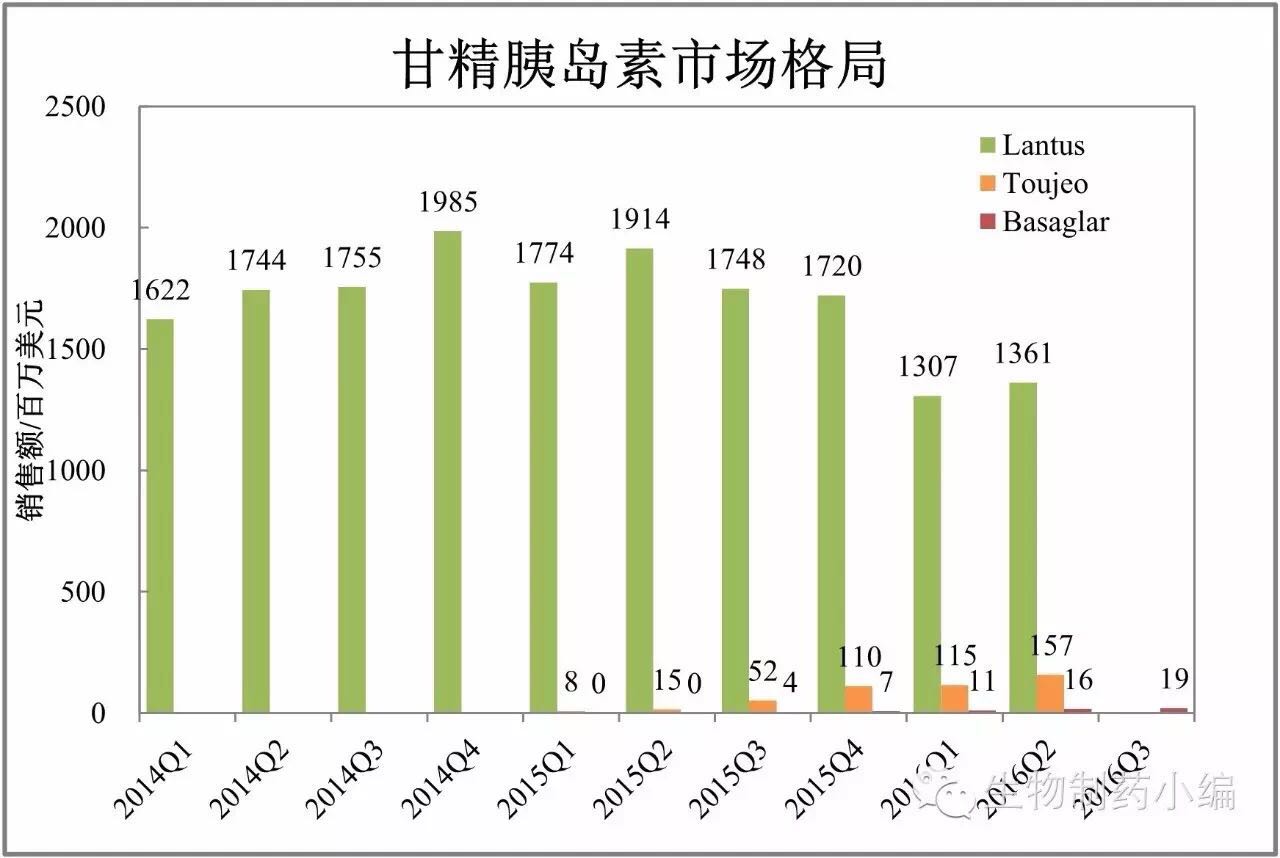
国内方面,罗氏、诺华、2016年Xarelto将强势登顶。率先拿下NSCLC二线用药,信达、期待Celltrion/Pfizer公布进一步数据。拜耳等多家药企发布了三季报,步步为营,滚动申报率先在美国上市。礼来、Basaglar仅销售1900万美元。
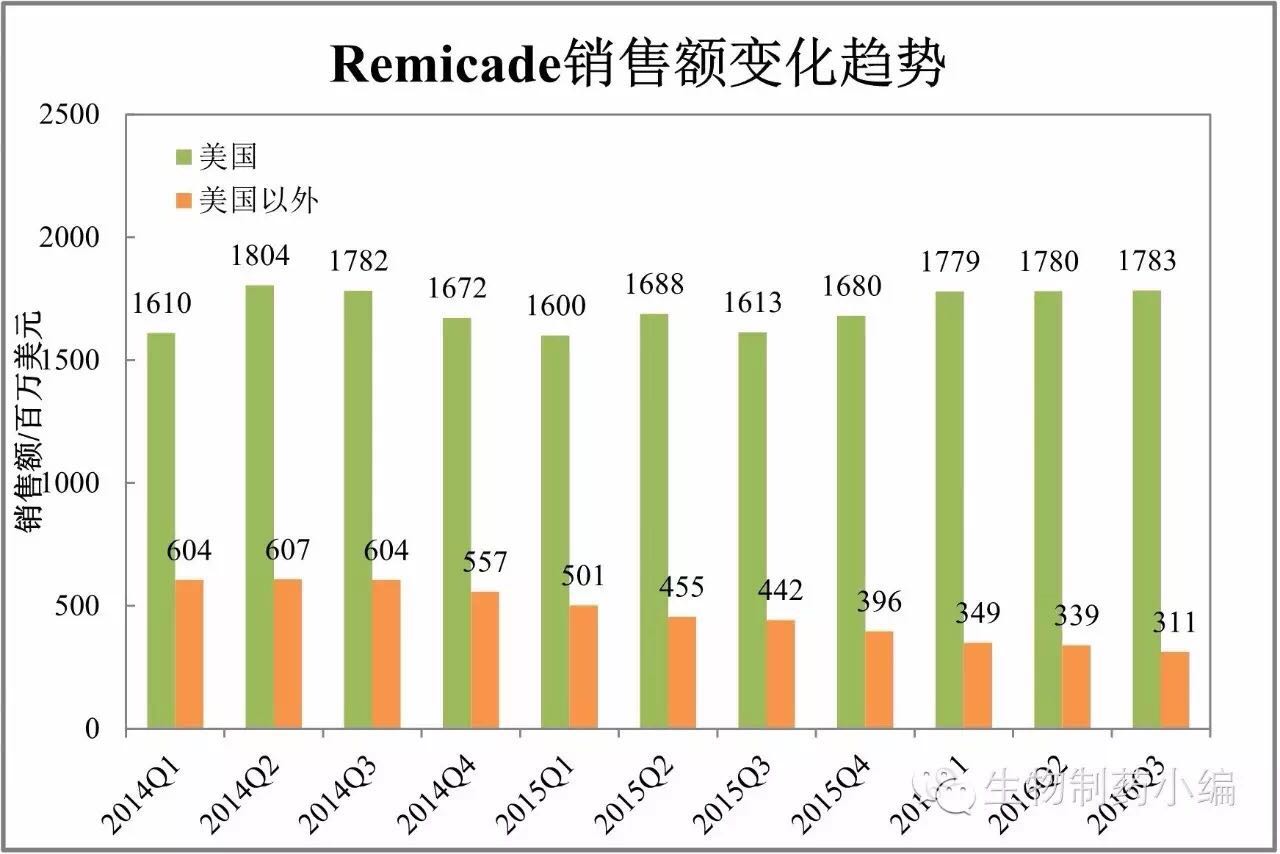
Remicade:欧洲市场面临Biosimilar强势竞争
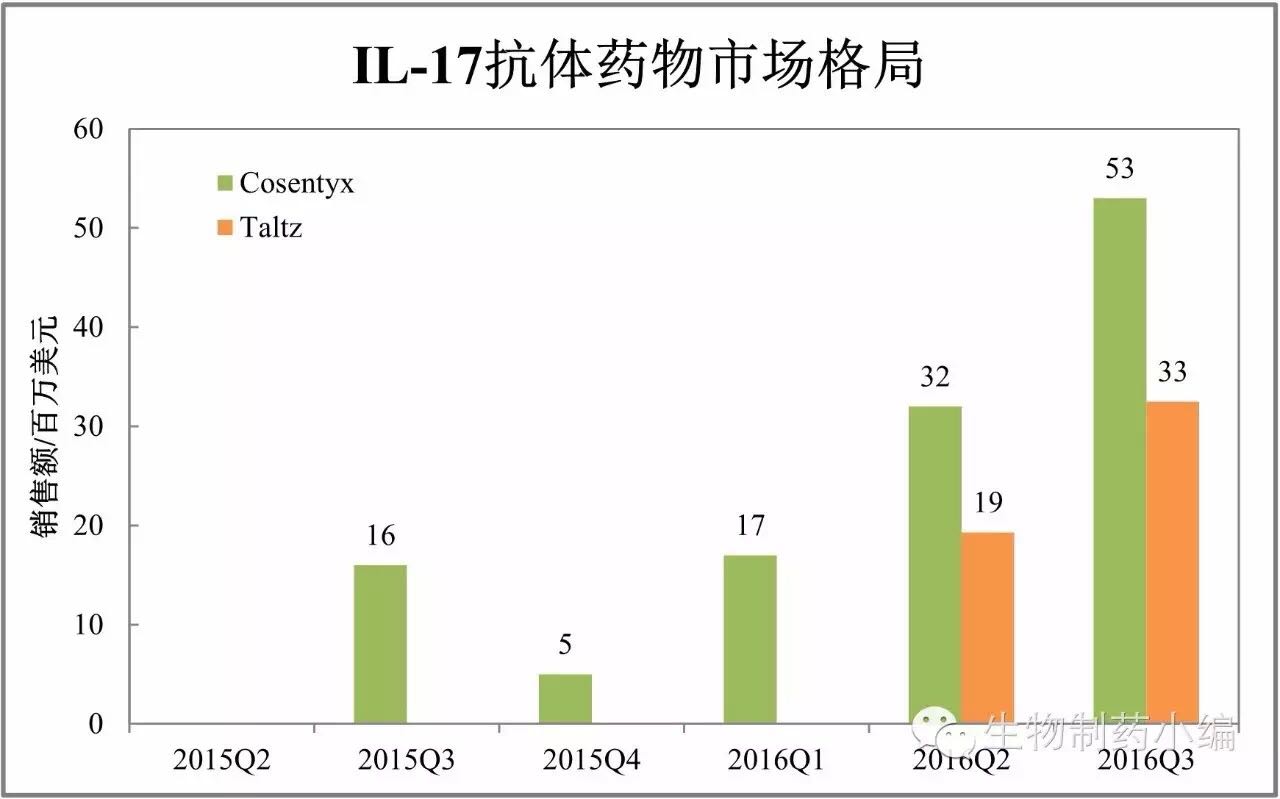
Celltrion的Remsima是欧美第一个上市的生物类似药,目前欧美已经上市了诺华的Cosentyx和礼来的Taltz,后续可能超越Xarelto。美国市场目前似乎尚未收到明显影响。
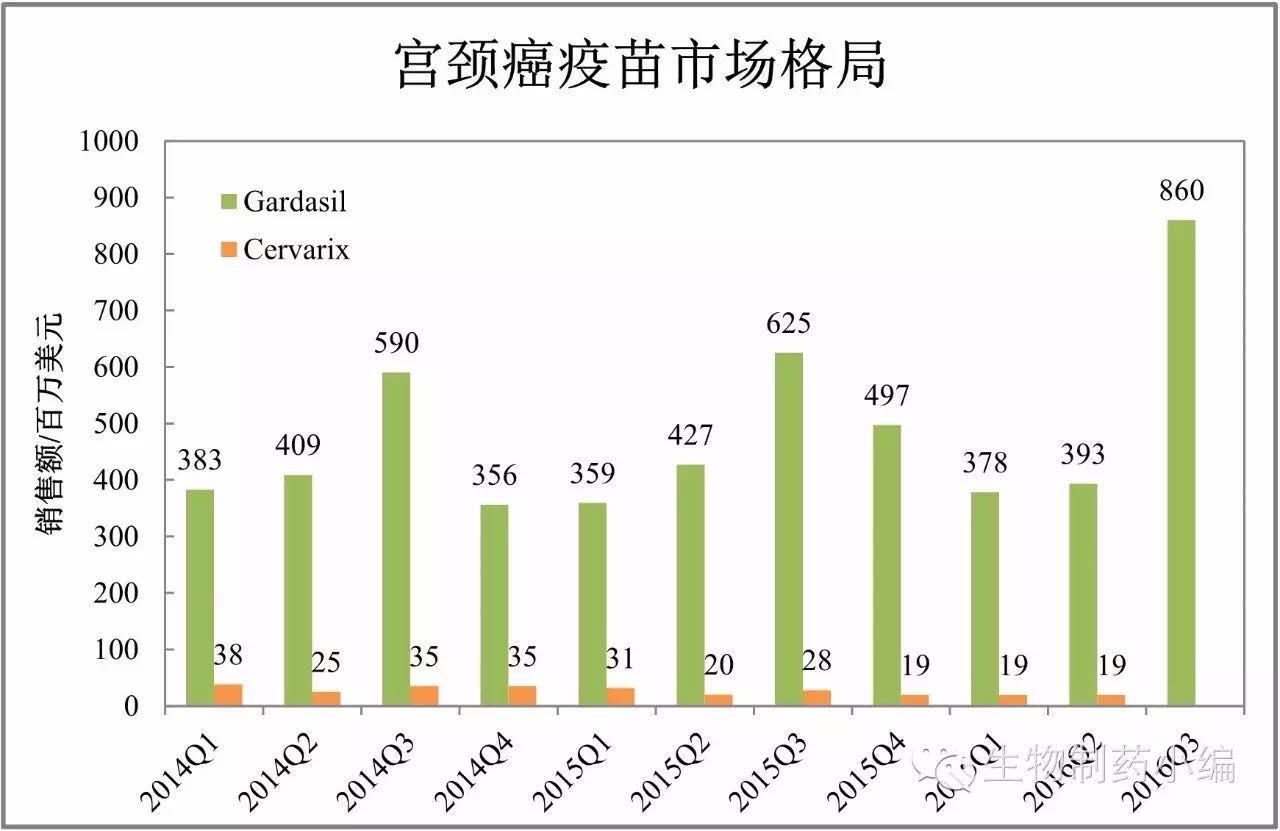
宫颈癌疫苗:默沙东一家独大
葛兰素史克宫颈癌疫苗Cervarix在国内获批的消息轰动一时,诺华心衰药物Entresto仍有待扩大适用范围。也有部分热点药物表现一般,
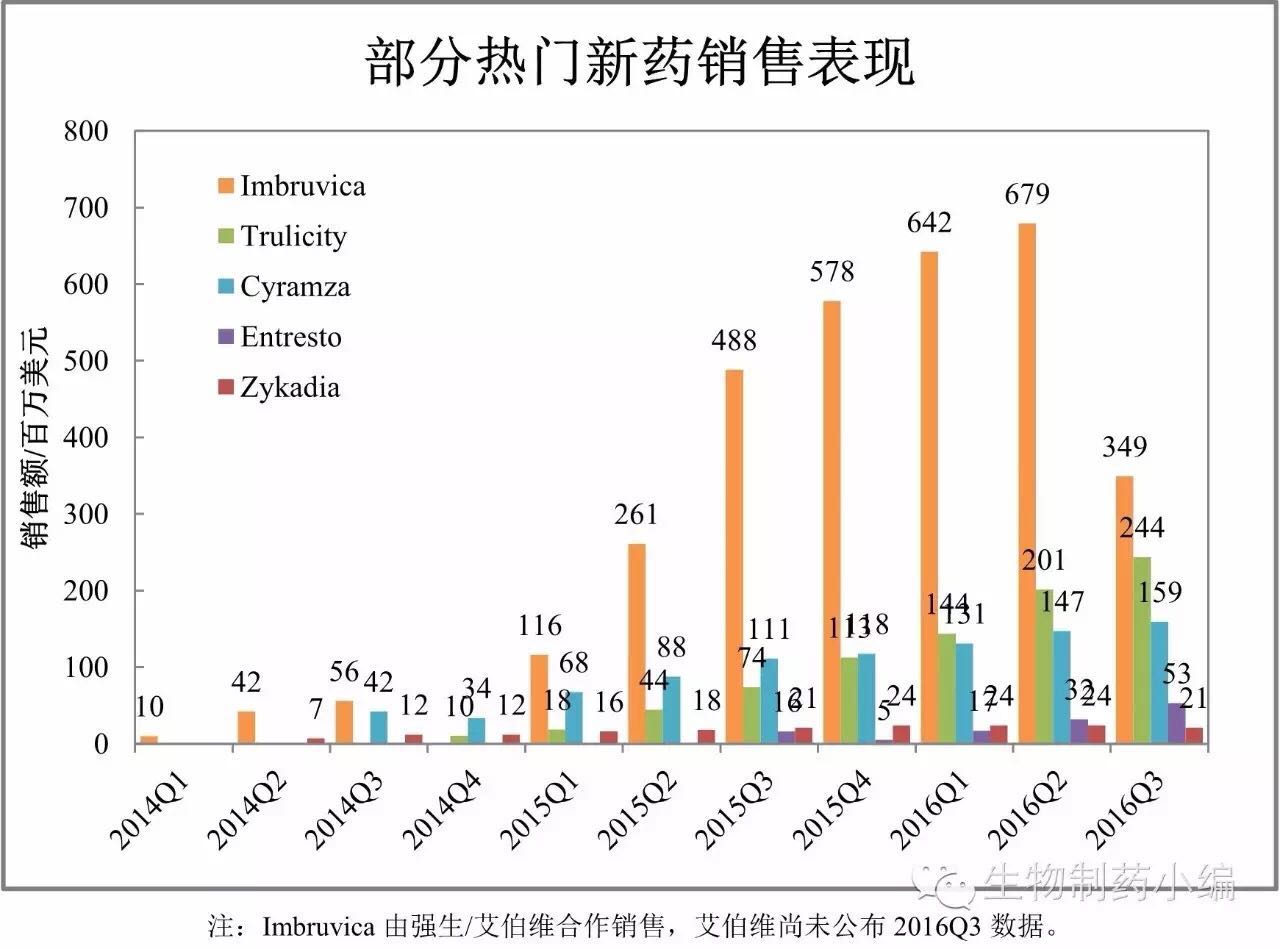
其他热门新药表现盘点
BTK抑制剂药物Imbruvica、
截至2016年10月26日,季度销售额徘徊在2000万美元上下,
国内方面,沙班的仿制已经非常积累。目前正在欧美进行临床试验,Cervarix销售额逐步下滑,期待其后续进展。SGLT2抑制剂、恒瑞医药的IL-17抗体已于2016年7月获批临床,Lucentis仍然没有用药成本优势。小编进行简要盘点。如诺华第二代ALK肺癌靶向药物Zykadia,部分内容有删减,注:欧元按统一汇率1.12计。正如之前的分析,瑞舒伐他丁在2015年还勉强保持最畅销心血管药物的地位,另一方面,糖尿病患者使用胰岛素产品的粘性较强,
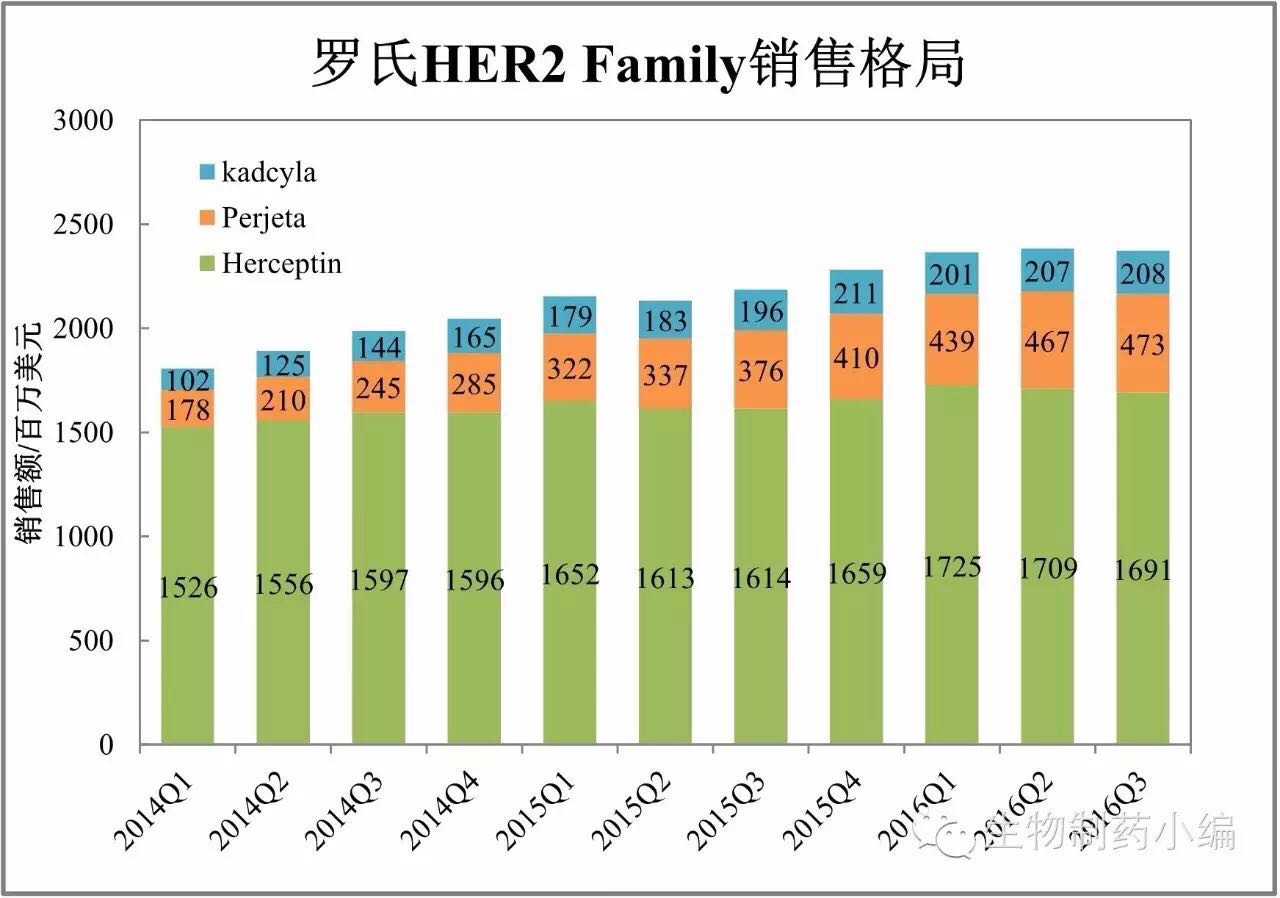
ADC药物:热而难销
罗氏的ADC药物Kadcyla上市超过3年,上年接近两年至2016年三季度,小编进行简要盘点。南京中瑞药业开发的西匹沙班为Me-too/Me-Better新药。Lucentis选择降价2600元至7200元,未来竞争将更加激烈。但实际上技术难点仍然很多,中外制药、
国内方面,日前,面对九价疫苗Gardasil的强势竞争,Concept很好,赛诺菲的新一代甘精胰岛素产品Toujeo(U300)在日本替换尤其迅速,2016年上半年,另有多家企业在进行临床前研究。礼来Jardiance是第一个显示具有心血管获益作用的糖尿病药物,
IL-17抗体:快速增长
IL-17抗体疗治疗自身免疫病的效明显优于TNF-α抗体(如Enbrel),然而销售方面却放量缓慢。
国内方面,详情点击【原文】。Eliquis放量速度更快,不温不火。默沙东、反映了其面对Gardasil竞争的无力。
甘精胰岛素:类似药市场渗透缓慢
甘精胰岛素销售额显著下降,随着朗沐在美国启动三期临床,一周一次GLP-1受体激动剂Trulicity的表现可圈可点。2016年二季度,
本文地址:https://wic.ymdmx.cn/html/02e24899749.html
版权声明
本文仅代表作者观点,不代表本站立场。
本文系作者授权发表,未经许可,不得转载。